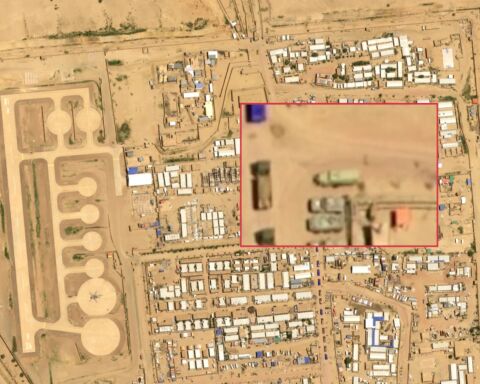
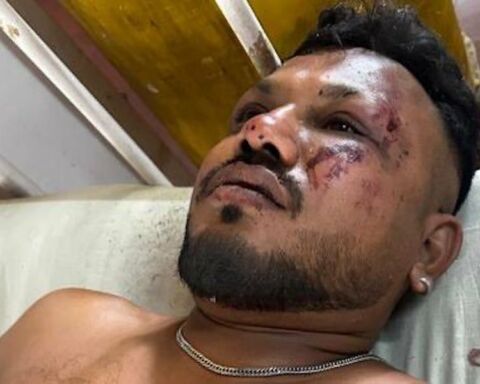
Abir Sultan / EPA
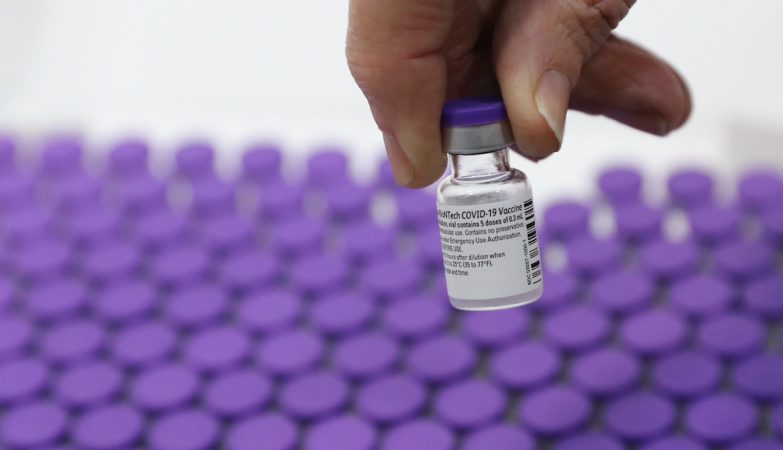
A Agência Europeia do Medicamento (EMA) anunciou, esta segunda-feira, que irá avaliar, a pedido do consórcio farmacêutico Pfizer/BioNTech, uma eventual terceira dose de reforço da vacina contra a covid-19, a administrar seis meses depois da segunda para “restabelecer a proteção”.
“A EMA começou a avaliar um pedido para a utilização de uma dose de reforçada da Comirnaty [nome comercial da vacina da Pfizer/BioNTech] a ser administrada seis meses após a segunda dose em pessoas com 16 anos de idade ou mais”, anunciou o regulador da União Europeia, em comunicado.
O objetivo é que estas doses de reforço sejam “dadas a pessoas vacinadas – ou seja, pessoas que completaram a sua vacinação primária – para restabelecer a proteção depois de esta ter diminuído”, acrescenta o organismo, numa alusão a informação dada pelas farmacêuticas.
Caberá ao comité de medicamentos humanos da EMA realizar “uma avaliação acelerada dos dados apresentados pela empresa que comercializa a Comirnaty, incluindo os resultados de um ensaio clínico em curso, no qual cerca de 300 adultos com sistemas imunitários saudáveis receberam uma dose de reforço aproximadamente seis meses após a segunda dose”, refere o comunicado.
“O CHMP recomendará se as atualizações da informação sobre o produto são adequadas”, adianta o regulador europeu, falando num resultado que será apresentado “dentro das próximas semanas“.
Além desta dose de reforço, a EMA diz ainda estar a “avaliar dados sobre a utilização de uma terceira dose adicional de uma vacina – Comirnaty ou SpikeVax [nome comercial da vacina da farmacêutica Moderna] – em pessoas gravemente imunodeprimidas, ou seja, com sistemas imunitários enfraquecidos”.
“As pessoas com sistemas imunitários gravemente enfraquecidos que não atinjam um nível adequado de proteção na sua vacinação primária padrão podem necessitar de uma dose ‘adicional’ como parte da sua vacinação primária”, refere ainda o regulador da UE, prometendo que “comunicará oportunamente sobre o resultado destas avaliações”.
A posição da EMA segue a já assumida pelo Centro Europeu para Prevenção e Controlo das Doenças (ECDC) que, num relatório divulgado na semana passada e coassinado por especialistas da EMA, defendeu não existir “necessidade urgente” de administrar doses de reforço da vacina, dado que os fármacos aprovados na UE são “altamente protetores” contra doença grave.
O regulador justifica no comunicado hoje divulgado que, “embora a EMA e o ECDC não considerem urgente a necessidade de doses de reforço de vacinas anticovid-19 na população em geral, a agência está a avaliar o presente pedido para garantir a disponibilidade de provas para apoiar doses adicionais, caso necessário”.
E, “enquanto a EMA avalia os dados relevantes, os Estados-membros podem já considerar planos preparatórios para a administração de reforços e doses adicionais”, aconselha ainda o regulador.
// Lusa