Equipa na Florida tenta criar um animal de grande porte só a partir de células estaminais — sem óvulos, sem espermatozoides, sem conceção. É um processo promissor, mas com muitos obstáculos pela frente.
Utilizando sémen de touros de elite, muitos bovinos de carne e de leite são submetidos a inseminação artificial. São mais de um milhão de tentativas de fertilização in vitro (FIV) por ano, metade das quais com lugar na América do Norte.
Há muitos obstáculos para este campo na reprodução de bovinos, mas a tecnologia já está disponível.
Recentemente, estudantes a colaborar no laboratório do biólogo reprodutor Zongliang Jiang, na Florida, recolheram um espécime danificado da vaca n.º 307. O conteúdo do útero foi retirado para um balde e o estudante responsável percebeu: “é qualquer coisa, mas é difícil dizer” o quê.
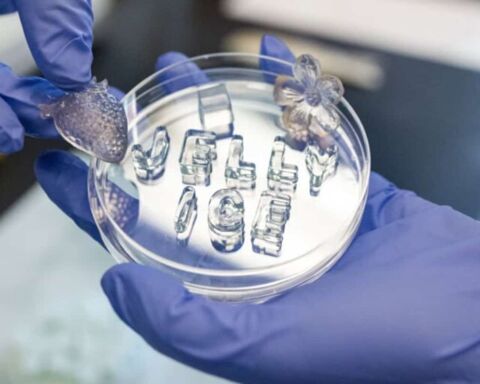
Nesse dia, os estudantes transportaram o que pareciam ser estruturas embrionárias intactas numa placa de Petri. Estas estruturas, que se assemelham a vermes ou à pele de pequenas cobras, eram na realidade embriões de bovinos com duas semanas de idade.
A ideia passa por tentar criar um animal de grande porte só a partir de células estaminais — sem óvulos, sem espermatozoides, sem conceção.
Embora exteriormente normais, estes embriões revelam uma desordem interna significativa ao exame microscópico após coloração química.
O disco embrionário e as células da placenta estão presentes, mas estão mal organizados, o que leva Jiang a hesitar em rotulá-los como embriões devido às incertezas quanto à sua saúde.
“O gado é mais difícil”, diz Jiang. “Mas nós temos toda a tecnologia. Eu ainda não lhes chamaria embriões, porque ainda não podemos dizer se são saudáveis ou não”, afirma. “As linhagens estão lá, mas estão desorganizadas”, explica, citado pelo MIT Technology Review.
Blastoides como substituto da clonagem
O laboratório de Jiang é também pioneiro na utilização de blastoides, que são produzidos colocando células estaminais em tubos estreitos onde tentam rapidamente formar estruturas embrionárias.
Este método pode potencialmente aumentar a escala para produzir centenas de milhares de blastoides, posicionando-o como uma alternativa mais simples às técnicas tradicionais de clonagem, que requerem ovos e técnicos especializados.
“Podemos gerar centenas de milhares de blastoides. Portanto, é um processo industrial”, diz. “É muito simples”, garante o biólogo.
Apesar do seu imenso potencial, os blastoides ainda não são um substituto funcional para a clonagem — têm expressões genéticas anormais que levam ao seu fracasso. A sua aparência é frequentemente distorcida, faltando-lhe a precisão e a clareza esperadas de um desenvolvimento embrionário bem sucedido.
“Os embriões parecem borrados, como se alguém os tivesse esculpido com farinha de aveia ou plasticina. Não é a coisa bonita que está à espera. Faltam os pormenores mais finos”, diz Cody Kime, diretor de I&D da Trans Ova Genetics, em Sioux Center, Iowa, que confessa que recebeu muitas críticas quando começou a clonar milhares de porcos e centenas de bovinos premiados.
“Diziam ‘oh, isto não vai funcionar’ e que isto é de alto risco e baixa eficiência”, recorda: “Mas, para mim, isto mudaria todo o programa de criação.”