Sanofi Pasteur / Flickr
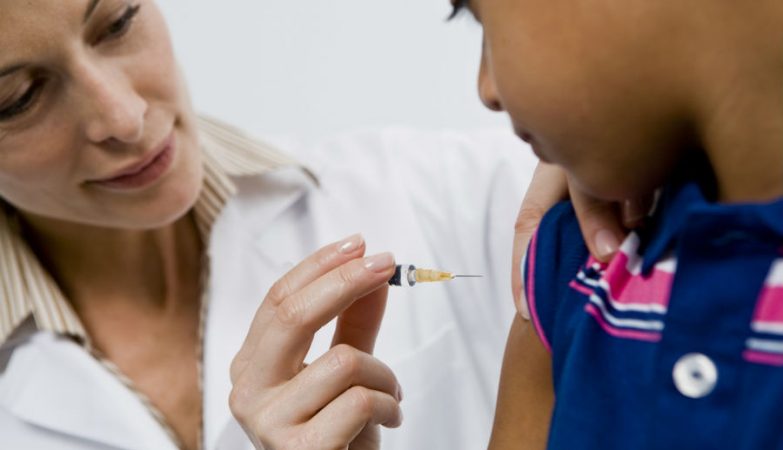
A Food and Drug Administration (FDA) autorizou a administração da vacina contra a covid-19 da Pfizer a crianças de 12 a 15 anos. A imunização de jovens pode arrancar já esta quinta-feira.
Agora que a Food and Drug Administration (FDA) concedeu a autorização de uso de emergência da vacina, os Centros de Controle e Prevenção de Doenças reunir-se-ão para recomendar como será usada nesta faixa etária, explica o jornal britânico The Independent.
Os pais terão permissão para vacinar os filhos assim que o CDC aprovar essa recomendação.
A decisão de que a vacina é segura para adolescentes permitirá que milhões de norte-americanos sejam vacinados, o que é essencial para que o país alcance a imunidade de grupo.
A decisão era aguardada com grande expectativa pelos pais, professores e profissionais de saúde antes das férias de verão e do novo período letivo que começa ainda este ano.
A expansão da FDA da autorização de uso de emergência para a vacina Pfizer-BioNTech para incluir adolescentes de 12 a 15 anos de idade é um passo significativo na luta contra a pandemia de covid-19”, disse Janet Woodcock, comissária em exercício da FDA. “A ação de hoje permite que uma população mais jovem seja protegida da covid-19, aproximando-nos do regresso à normalidade e do fim da pandemia”.
“Os pais e responsáveis podem ter a certeza de que a agência realizou uma revisão rigorosa e completa de todos os dados disponíveis, como fizemos com todas as nossas autorizações de uso de emergência da vacina covid-19”, garantiu Woodcock.
De acordo com a CNN, a imunização dos adolescentes pode arrancar já esta quinta-feira.
O Comité Consultivo em Práticas de Imunização dos Centros para Controle e Prevenção de Doenças dos Estados Unidos agendou uma reunião de emergência para quarta-feira, possivelmente, para votar a recomendação do uso da vacina. Depois disso, espera-se que a diretora do CDC, Rochelle Walensky, dê a sua aprovação final, após a qual os estados poderão começar a administrá-la.
“Suporíamos que poderia ser assim na quinta-feira”, disse Peter Marks, diretor do Centro de Avaliação e Pesquisa Biológica da FDA, numa conferência de imprensa. “Quinta-feira, certo”, acrescentou Woodcock.
As crianças quase não foram afetadas pela covid-19. Das 581 mil mortes por covid-19 nos Estados Unidos, apenas 300 ocorreram em pessoas com menos de 18 anos.
Porém, a FDA disse que esse número é maior do que o número de crianças que morreriam de gripe todos os anos.
O FDA tomou a decisão com base num ensaio da Pfizer com cerca de 2.300 jovens de 12 a 15 anos, em que os investigadores descobriam que o grupo realmente tinha uma resposta imunológica mais forte do que os jovens adultos.
“Ter uma vacina autorizada para uma população mais jovem é um passo crítico para continuar a diminuir o imenso fardo de saúde pública causado pela pandemia de covid-19″, disse Marks.
“Com a ciência a guiar o nosso processo de avaliação e tomada de decisão, a FDA pode garantir ao público e à comunidade médica que os dados disponíveis atendem aos nossos padrões rigorosos para apoiar o uso de emergência desta vacina na população adolescente de 12 anos de idade ou mais.”
Vacinar crianças é possibilidade na Europa?
Em declarações ao jornal Público, Miguel Prudêncio, do Instituto de Medicina Molecular da Faculdade de Medicina de Lisboa, disse acreditar que a Agência Europeia do Medicamento (EMA) não vai fazer uma “transposição direta e imediata” da decisão da FDA, considerando previsível que sejam solicitados “dados adicionais e esclarecimentos sobre a forma como o estudo foi conduzido”.
“Estou em crer que os Estados Unidos, neste momento, podem dar-se ao luxo de camadas de população que não são de risco elevado, porque já têm uma cobertura vacinal da população adulta muito significativa. Julgo que na Europa ainda temos um caminho a percorrer antes de pensarmos em vacinar pessoas com um risco baixíssimo”, considerou.
Por outro lado, tendo em conta o historial de decisões, Miguel Castanho, também do instituto de Medicina Molecular da Universidade de Lisboa, considera provável que a decisão da EMA não seja muito diferente da adotada pela FDA.
“Espera-se que seja feito um pedido às autoridades europeias. Normalmente, os tipos de análise são semelhantes de um lado e de outro. É muito provável que, na Europa, também venha a acontecer. Não é obrigatório, longe disso, mas os critérios de avaliação têm semelhanças, não se espera uma diferença radical”, disse.
“A vacinação das crianças tem, porventura, mais impacto em termos comunitários pela redução na transmissão do vírus, do que propriamente na proteção das crianças vacinadas — que, à partida, não são um grupo que desenvolva tendencialmente formas mais graves da doença. De uma forma muito simplista, a grande vantagem é reduzirmos substancialmente a transmissão nesse grupo. Se a vacina impedir a infeção, evidentemente também impede a transmissão”, rematou.
Coronavírus / Covid-19
-
31 Março, 2024 Dos 7 aos 700 milhões: os novos números da COVID-19
-
4 Fevereiro, 2024 O fim do mundo: 6 teorias populares















